近日,湖北大学生命科学学院、省部共建生物催化与酶工程国家重点实验室李珊珊/余希岚团队最新研究成果“Metabolic regulation of telomere silencing by SESAME complex-catalyzed H3T11 phosphorylation(《细胞代谢通过SESAME复合物催化的H3T11磷酸化调控端粒沉默》)”,发表在《自然·通讯》(Nature Communications)(IF: 12.121)。团队研究生张世豪和余希岚教授为该论文共同第一作者,李珊珊教授为该论文通讯作者,湖北大学为唯一通讯单位(图1)。

图1 文章首页
端粒是染色体两端的“保护帽”,对于调控细胞衰老、肿瘤发生等非常重要。端粒具有典型的异染色质结构,对于维持染色体的稳定性和抵抗环境压力具有非常重要的作用。近来研究发现,端粒结构受到内在与外部环境的调控,比如营养缺乏、衰老等。然而,在这些压力条件下,端粒异染色质动态调节的分子机制尚不知晓。
SESAME复合体是李珊珊教授于2015年鉴定的一种由糖代谢酶组成的蛋白酶复合体,以丙酮酸激酶为催化亚基,通过磷酸化组蛋白H3T11来调控基因表达和增强细胞抵抗氧化压力的能力。在该项研究中,李珊珊教授研究团队从SESAME在染色体上的结合模式入手,发现SESAME可通过磷酸化端粒附近的组蛋白H3T11来维持SIR(沉默复合物)在端粒的结合并阻止Sir2蛋白出核被降解。同时,SESAME催化的H3pT11可直接抑制自噬相关基因的表达,进一步阻止了自噬介导的Sir2降解。本研究还发现在衰老过程中,SESAME复合物的活性下降,H3T11磷酸化相应地下降,导致自噬升高,Sir2被降解以及端粒异染色质结构的破坏,最终加快细胞的衰老进程(图2)。该研究揭示了在衰老过程中,糖代谢调控端粒异染色质结构的表观遗传学机制,为代谢干预衰老提供了重要的理论依据。
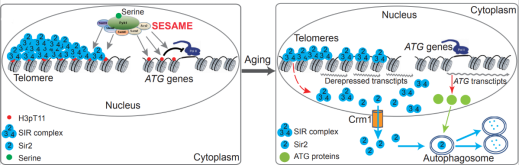
图2 SESAME复合物调控衰老过程中端粒结构的分子机制。
李珊珊教授和余希岚教授团队一直从事糖代谢调控衰老与肿瘤发生的表观遗传学研究。自2015年底加盟湖北大学生命科学学院以来,以湖北大学为第一通讯单位在Nature Communications (IF: 12.121)、Nucleic Acids Research (2篇,IF=11.502)、Oncogene (IF=7.971)等国际权威期刊上发表多篇高水平文章,并获得国家自然科学基金面上项目、青年项目、湖北省杰青项目等多项国家级和省部级科研项目的支持。